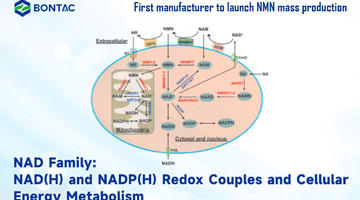
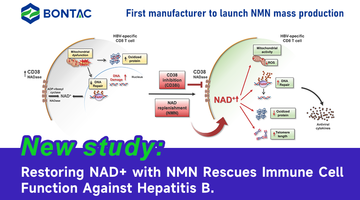
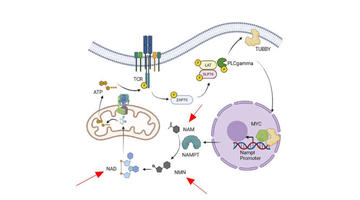
Nowe badanie: Przywrócenie NAD + za pomocą NMN ratuje funkcję komórek odpornościowych przeciwko wirusowemu zapaleniu wątroby typu B
Wyróżnić: W przewlekłym zakażeniu HBV podwyższona produkcja ROS wiąże się z wysokim uszkodzeniem DNA w limfocytach T CD8 specyficznych dla HBV
- Reakcja na uszkodzenie DNA jest dysfunkcyjna
- Regulacja w górę CD38 i trwała aktywacja polimeraz poli-ADP-rybozy (PARP)przyczynianie się do zużycia NAD
- wyczerpanie NAD utrzymuje i wzmacnia dysfunkcje komórkowe w wyczerpanym T specyficznym dla HBVKomórek
-Uzupełnianie NAD może przywrócić funkcję limfocytów T
Przewlekłe wirusowe zapalenie wątroby typu B (CHB) jest uporczywą infekcją wirusową, która dotyka miliony ludzi na całym świecie. Infekcja może spowodować poważne uszkodzenie wątroby, raka wątroby, a ostatecznie śmierć. Jedną z cech charakterystycznych zakażenia CHB jest wyczerpanie specyficznych dla wirusa limfocytów T CD8, które są niezbędne do usunięcia wirusa. Podwyższony poziom reaktywnych form tlenu (ROS) pochodzących z dysfunkcyjnych mitochondriów może powodować zwiększone utlenianie białek i uszkodzenie DNA w wyczerpanych limfocytach T CD8 specyficznych dla wirusa.Badacz wykazał, w jaki sposób zastosowanie mononukleotydu nikotynamidu (NMN) i dinukleotydu nikotynoamidoadeninowego (NAD) może potencjalnie przywrócić funkcję wyczerpanych limfocytów T CD8 w układzie CHB.
Mechanizm wyczerpania limfocytów T CD8 w CHB
Badania wykazały, że wyczerpanie limfocytów T CD8 u pacjentów z CHB jest związane z wadliwymi procesami naprawy DNA, w tym parylacją zależną od NAD. Wyczerpanie NAD jest wskazywane przez nadekspresję CD38, głównego konsumenta NAD, oraz przez znaczną poprawę mechanizmów naprawy DNA, funkcji mitochondriów i proteostazy poprzez suplementację NAD, co może również poprawić specyficzną dla HBV przeciwwirusową funkcję limfocytów T CD8. Sugeruje to, że wiele połączonych ze sobą defektów wewnątrzkomórkowych, w tym skracanie telomerów, jest przyczynowo związanych z wyczerpaniem NAD, które jest podobne do procesu starzenia się komórek.

Rola CD38 w wyczerpaniu limfocytów T CD8
CD38 został uznany za głównego konsumenta NAD, a jego nadekspresja wiąże się z wysokim spożyciem NAD i późniejszym wyczerpaniem oraz ze zmienioną funkcją mitochondriów. U starszych myszy nadekspresja CD38 wiązała się z niskim potencjałem błony mitochondrialnej i zwiększoną zależnością od glikolizy, cech metabolicznych wspólnych dla limfocytów T CD8 specyficznych dla HBV w CHB. Nadekspresja CD38 może być przyczynowo związana z niedoborem NAD w wyczerpanych limfocytach T CD8 specyficznych dla HBV.

Rola NAD w funkcji limfocytów T CD8
NAD jest niezbędnym koenzymem, który odgrywa kluczową rolę w utrzymaniu homeostazy energetycznej, naprawie DNA i sygnalizacji redoks. Przywrócenie wewnątrzkomórkowych poziomów NAD może poprawić funkcje mitochondriów i proteostazy, a tym samym przywrócić funkcję wyczerpanych limfocytów T CD8 w CHB. Ponadto suplementacja NAD może również przywrócić mechanizmy naprawy DNA i poprawić specyficzną dla HBV przeciwwirusową funkcję limfocytów T CD8.
Wyczerpanie limfocytów T CD8 jest główną przeszkodą w usuwaniu przewlekłych infekcji wirusowych, w tym CHB. Zastosowanie prekursora NAD NMN i suplementacji NAD wykazało obiecujące wyniki w przywracaniu funkcji wyczerpanych limfocytów T CD8 u pacjentów z CHB. Nadekspresja CD38 i późniejsze wyczerpanie NAD są głównymi czynnikami przyczyniającymi się do wyczerpania limfocytów T CD8 u pacjentów z CHB.

Dlatego korekta tych rozregulowanych funkcji wewnątrzkomórkowych przez suplementację NAD stanowi obiecującą potencjalną strategię terapeutyczną dla przewlekłego zakażenia HBV. Potrzebne są dalsze badania w celu zbadania pełnego potencjału NMN i NAD w leczeniu CHB.